Laufvogel-Evolution, Unfruchtbarkeit und Vererbung von Verhalten
Der Newsletter Epigenetik 31 ist erschienen



Heute erscheint die 31. Ausgabe des Newsletter Epigenetik. Dieser unabhängige, seit dem Jahr 2010 alle drei bis sechs Monate publizierte Newsletter fasst die wichtigsten Neuigkeiten aus einem der spannendsten Forschungsgebiete unsere Zeit zusammen: der Epigenetik. Ich bin Autor und Herausgeber des Newsletters, und ich schreibe hier in diesem RiffReporter-Online-Magazin Erbe&Umwelt zu diesem und einigen anderen Themen. Unterstützt wird der Newsletter Epigenetik durch ein achtköpfiges Gremium aus Mediziner*innen und Forscher*innen, die mich als Mitherausgeber beraten. Den gesamten Newsletter sowie Informationen über die Mitherausgeber*innen und ein Archiv mit sämtlichen bisher erschienenen Beiträgen, finden Sie auf www.newsletter-epigenetik.de.
Möchten Sie den Newsletter Epigenetik unterstützen, abonnieren Sie einfach das Magazin Erbe&Umwelt und erhalten so ganz nebenbei auch noch Zugang zu den exklusiven Hintergrundartikeln, die dort über Epigenetik aber auch zu Themen wie Schlafforschung und Biorhythmik erscheinen. Als kostenlosen Service gibt es zudem die Erbe&Umwelt-News, die zwei bis vier Mal pro Monat Neuigkeiten vermeldet rings um Erbe&Umwelt, den Autor Peter Spork sowie seine kommenden öffentlichen Auftritte.
In der neuen Ausgabe des Newsletter Epigenetik lesen Sie unter anderem darüber, wie lebenslanger Sport unsere Zellen epigenetisch so umprogrammiert, dass wir langsamer altern. Und sie lernen eines der ambitioniertesten biomedizinischen Forschungsprojekte Europas kennen, LifeTime genannt. Zu beiden Themen finden Sie – wie auch zu einigen anderen Beiträgen im Newsletter – im exklusiven, nur für Abonnenten oder nach einer Einmalzahlung voll sichtbaren Angebot von Erbe&Umwelt ausführliche Hintergrundartikel,
Für einen Blick auf das Inhaltsverzeichnis des Newsletter Epigenetik 31 klicken Sie bitte weiter oben auf das Titelbild. Es zeigt übrigens vier Arten von Laufvögeln: Strauß, Nandu, Moa (ausgestorben) und Steißhuhn. Diese interessanten Tiere haben mindestens drei Mal unabhängig voneinander ihre Flugfähigkeit verloren. Dass bei dieser konvergenten Evolution auch die Epigenetik ein gewichtiges Wörtchen mitgeredet hat, erfahren Sie gleich in der ersten hier eingestellten Meldung. Es ist inzwischen nämlich eine schöne Tradition, dass ich Ihnen sozusagen als Appetithäppchen an dieser Stelle drei der aktuellen Meldungen serviere. Den gesamten Newsletter können Sie auf www.newsletter-epigenetik.de herunterladen. Dort können Sie sich auch für den Bezug der PDF-Ausgabe per E-Mail anmelden.

Epigenetische Regulation hilft Laufvögeln bei konvergenter Evolution
Evolutionsbiologen sind immer wieder fasziniert von der Existenz so genannter konvergenter Entwicklungen. Das Auge wurde ebenso mehrfach im Tierreich entwickelt wie das Fliegen oder die zu Grabwerkzeugen umfunktionierten Vorderbeine bei Maulwürfen und Maulwurfsgrillen. Ein spannendes Beispiel für konvergente Evolution bei vergleichsweise nahe verwandten Arten ist der mehr oder weniger vollständige Verlust der vorderen Extremitäten und damit der Flugfähigkeit bei verschiedenen Laufvogelarten. Strauße, Nandus, Emus, Kasuare, Kiwis oder auch die ausgestorbenen Moas können oder konnten zwar alle nicht fliegen, das Merkmal ist in ihrer Gruppe aber mindestens drei, vielleicht sogar sechs Mal unabhängig voneinander entstanden.
Jetzt hat ein internationales Forscherteam sich den Knochenbau sowie die Genetik und Epigenetik der Laufvögel und einiger verwandter flugfähiger Vögel genauer angesehen und klare Hinweise darauf gefunden, dass auch artspezifische Veränderungen der Genregulation konvergente Entwicklungen bewirken können. So fanden die Biologen anders als frühere Gruppen keine Hinweise darauf, dass Mutationen in bestimmten Genen die Rückbildung der Flügel ausgelöst haben. Stattdessen sind eindeutig mehrere so genannte Enhancer betroffen, also epigenetisch aktive Elemente, die die Ablesefrequenz benachbarter Gene heraufregulieren sobald ein passendes Protein (Transkriptionsfaktor) an sie bindet.
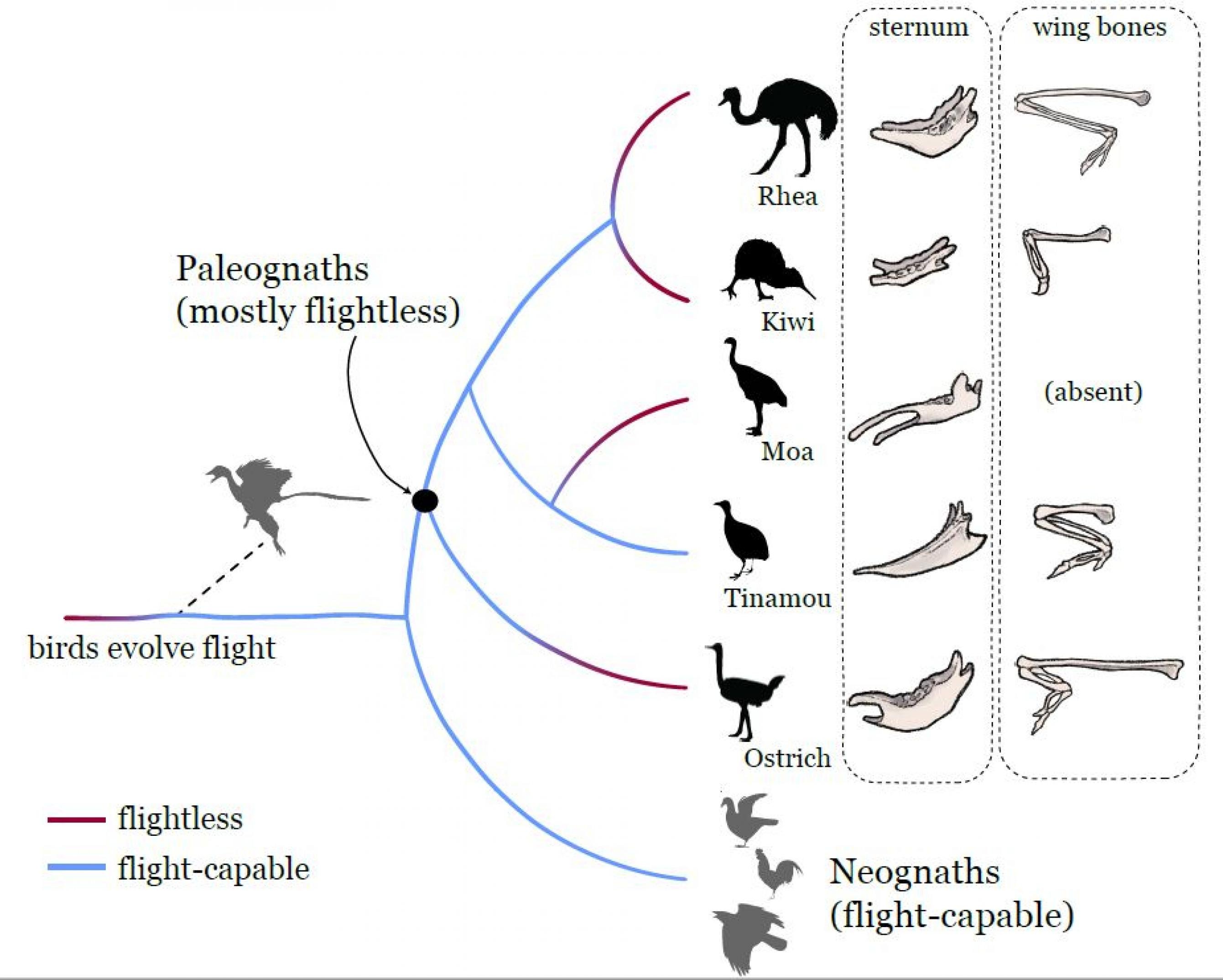
Mit Hilfe einer Atac-seq genannten Methode identifizierten die Forscher während der entscheidenden Entwicklungsphase der Jungvögel all jene Stellen im Erbgut, an denen die DNA epigenetisch besonders leicht zugänglich war. Es zeigte sich, dass hier auch Enhancer liegen, die das Wachstum der Flügel anregen, indem sie die passende Genaktivität verstärken, und sich noch dazu zwischen flugfähigen und flugunfähigen Vögeln systematisch unterscheiden. Vor allem aber: Bei den geflügelten Vögeln funktionierte mindestens einer dieser Enhancer gut, während er bei den flügellosen Vögeln nicht mehr richtig arbeitete. Die Genregulation steuere zur konvergenten Evolution der Laufvögel offenbar eine „substantielle Komponente bei“, lautet das Fazit der Forscher.
Epigenetik der Unfruchtbarkeit
Zwei neue Studien beschäftigen sich mit möglichen epigenetischen Auslösern von weiblicher Unfruchtbarkeit. Shijian Lv von der Universität von Shanghai, China, und Kolleg*innen entdeckten Auffälligkeiten bei Frauen, die aus bislang unbekannten Gründen immer wieder Fehlgeburten haben. Dabei zeigte sich, dass die Plazentazellen solcher Frauen ungewöhnlich niedrige Mengen des epigenetisch aktiven Enzyms EZH2 produzieren. Indem dieses Enzym die Genregulation der Zellen verändert, scheint es die Einnistung des Embryos erst möglich zu machen. Fällt die epigenetische Umprogrammierung zu schwach aus, kann der Embryo sich nicht einnisten und es kommt zur Fehlgeburt. Für diese These spricht auch, dass das Sexualhormon Progesteron, das bereits erfolgreich im Kampf gegen Fehlgeburten eingesetzt wird, den EZH2-Spiegel der Plazentazellen anhebt.
Das Team um Tae Hoon Kim von der Michigan State University, USA, untersuchte hingegen Frauen, die wegen einer Endometriose keine Kinder bekommen können. Bei diesem häufigen, sehr belastenden und schmerzhaften Leiden wächst Gewebe aus der Gebärmutter in den Eierstöcken. Warum eine Endometriose manchmal aber auch zu Unfruchtbarkeit führt, war bislang unklar. Die Forscher entdeckten nun bei jenen Frauen mit einer endometriosebedingten Unfruchtbarkeit eine epigenetische Besonderheit: Die Gebärmutterzellen dieser Frauen produzieren ungewöhnlich geringe Mengen des epigenetischen Enzyms HDAC3 – eine Histondeacetylase, die Acetylgruppen von Histonproteinen entfernt und damit Gene weniger gut aktivierbar macht. In weiterführenden Experimenten mit Zellkulturen und Mäusen fanden die Forscher heraus, dass das Enzym offenbar Gene beeinflusst, die für die Bildung von Kollagenfasern wichtig sind. Ist zu wenig HDAC3 vorhanden, produziert die Gebärmutter demnach zu viel Kollagen, was das Einnisten des Embryos verhindert und zur Unfruchtbarkeit führt.
Würmer vererben ihr Verhalten
www.the-scientist.com/news-opinion/worm-parents-pass-on-behaviors-epigenetically-to-offspring-65988
Das Magazin The Scientist berichtet über zwei aufregende Studien bei Fadenwürmern Caenorhabditis elegans, die herkömmliche Vorstellungen von Vererbung ins Wanken bringen dürften. Danach geben die winzigen Tiere auch erworbene, im Nervensystem gespeicherte Verhaltensweisen an folgende Generationen weiter. Im ersten Experiment (Posner et al.: Cell 177, 13.06.2019) starben Würmer, weil sie giftige Bakterien gefressen hatten. Zuvor legten sie aber Eier ab, die bestimmte epigenetisch aktive nichtkodierende RNA enthielten. Diese Information genügte, um das Nervensystem der vier folgenden Wurm-Generationen so zu verändern, dass diese die giftigen Bakterien mieden. Bei weiteren Generationen verschwand das Verhaltensmuster wieder.
Im zweiten Experiment gingen Forscher der Frage nach, ob und wie epigenetische Informationen aus den Nervenzellen in die Eizellen gelangen können (Moore et al.: Cell 177, 13.06.2019). Die Forscher veränderten die Nervenzell-Genetik so, dass diese ein bestimmtes Muster nichtkodierender RNAs erzeugten, und staunten nicht schlecht, als das gleiche Muster in den Eizellen sowie in den Nervenzellen der folgenden drei Generation auftauchte. Die genauen Mechanismen der transgenerationellen Vererbung von Verhalten sind zwar noch völlig unklar. Auch weiß niemand, ob die Resultate auf uns Menschen übertragbar sind. Es dürfte dennoch sehr spannend werden, was in der Ecke der Fadenwurm-Forschung demnächst noch so alles publiziert wird.